Your privacy is very important to us. When you visit our website, please agree to the use of all cookies. For more information about personal data processing, please go to Privacy Policy.


辉大基因HG004 IND获NMPA批准,将开展中国首个国际多区域、多中心同一主方案的基因治疗药物临床试验
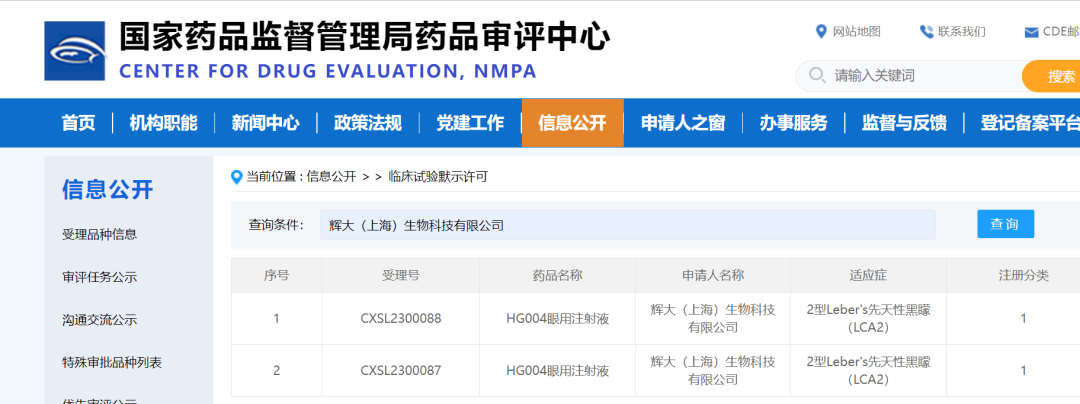
2023年4月18日,专注于基因治疗药物开发、处于临床阶段的全球性生物技术公司——辉大(上海)生物科技有限公司(简称“辉大基因”)宣布,其自主研发的首个眼科基因治疗药物HG004的临床试验申请(IND)已获得中国国家药品管理局药品审评中心(CDE)批准,标志着该候选药物正式全面进入国际多中心临床开发阶段。此前,HG004已在今年1月成功获得美国FDA的IND许可,以及3月获得美国FDA的孤儿药资格(ODD)认定。
辉大基因联合创始人兼首席执行官姚璇博士表示,“HG004的IND申请先后获得美国FDA与中国CDE的批准,是辉大基因研发进程中的重要里程碑,是对辉大团队卓越的创新研发能力的充分认可。同时,HG004的国际多区域、多中心主方案(Master Protocol)被FDA和NMPA的同时批准,也使得辉大成为中国第一家在基因治疗领域达成国际多区域、多中心同一主方案临床开发策略的基因治疗公司,极大地促进辉大迈向全球化的进程。在此,感谢公司成立运营至今四年来团队成员的齐心努力,以及合作伙伴和相关监管部门的鼎力支持,未来我们将全力以赴推进HG004的临床开发进程,并持续研究开发更多自主创新基因治疗产品,让更多安全有效的创新药物尽早惠及全球患者及家庭。”
辉大基因科学顾问委员会成员陆英明博士表示,“ HG004项目旨在开发一种一次性的非AAV2基因替代疗法,为全球因RPE65基因突变相关视网膜病变(IRD)导致的严重视力障碍或失明的儿童和成人患者提供治疗的手段。作为中国首个国际多区域、多中心同一主方案的眼科基因治疗药物,辉大基因团队将在全球临床开发中深入、全面地探索HG004的临床安全性、耐受性、疗效和持久性,以期为患者带来更优临床价值和更高产品质量的创新药物。”
“HG004注射液是一种新型眼科基因治疗药物,旨在用于治疗RPE65基因突变相关性视网膜病变,目前我们已获得高质量的临床前数据来支持即将开展的国际多区域、多中心临床试验。HG004的起始有效剂量(约1/25的载体剂量)远低于已批准的AAV2-hRPE65(LUXTURNA)基因治疗产品,并且需要注入视网膜的体积更小,这将大大减少AAV载体相关的免疫原性或人类的眼部不良事件的风险。”姚璇博士表示:“此前在中国上海新华医院进行的研究者发起的临床试验(IIT)中,取得了令人振奋的初步有效性结果,使用HG004的成人和儿童患者的视力得到了明显实质性的恢复(辉大基因眼科基因治疗候选药物HG004临床研究完成首例患者入组)。”
关于HG004国际多区域、多中心临床试验
HG004是一项多国、多中心、多队列、剂量探索性研究,将在RPE65视网膜病变成人及儿童患者中进行。在不同国家和区域将采用同一主方案,本研究的目的为评估HG004单次注射至52周的安全性、耐受性、有效性和长期临床持久性,主要终点包括不良事件、特定实验室检查和眼科检查。这项研究还将通过国际标准的多亮度移动测试(MLMT)来评估视觉功能,以及受试者将继续在HG004的长期随访研究中接受评估。
关于RPE65突变相关的遗传性视网膜疾病
遗传性视网膜营养不良(IRD)是一类由基因突变引起罕见致盲性疾病,已报道致病基因超过250个。其中,RPE65基因突变可能会导致Leber先天性黑蒙(LCA)、严重的早发性儿童视网膜营养不良(SECORD)、早发性严重视网膜营养不良(EOSRD)或视网膜色素变性(RP),即这些疾病都被认为是RPE65基因突变相关视网膜病变,代表同一疾病的表型连续体。RPE65基因突变相关视网膜病变通常发病于出生至5岁之间,主要临床表征包括夜盲(凝视伴严重夜盲症和眼球震颤)、进行性视野缺失和中心视力丧失。符合世界卫生组织(WHO)失明诊断标准(双等位基因RPE65突变)的患者比例随年龄增长而增加,40岁后达到100%。RPE65基因突变相关视网膜病变引起的严重和早期视力丧失,也可能会造成语言、社交和行为等其他功能的发育延迟。
关于辉大基因
辉大(上海)生物科技有限公司(下称“辉大基因”)成立于2018年,总部位于中国上海,并在美国新泽西设有办公室,是一家全球性的临床阶段生物技术公司,专注于设计和开发基于CRISPR技术的基因治疗药物,旗下员工近200人,其中研发团队占85%以上。自成立以来,辉大基因已完成来自中国专业医疗投资机构以及知名产业基金的四轮融资,并与多家国内顶级科研机构、医院达成深度合作。
辉大基因致力于通过各项在研药物管线满足全球患者的切实需求,长期目标是利用基因编辑技术治疗遗传病以及威胁人类健康的慢性疾病。研发管线涵盖眼科、听力、肌肉、中枢神经等多个领域,拥有多项全球领先水平的技术平台,涵盖从药物靶点筛选、药物优化、高效动物模型构建,到药效、毒理分析等临床前研发,再到药物工艺开发、生产转化CMC以及药品临床及注册申报的一体化研发能力。
辉大基因坚持以人为本,创新驱动,让基因治疗惠及千百万患者,致力成为全球领先的生物制药公司。
➣ 欲了解更多信息,请访问公司官网:
http://www.huidagene.com
或者在领英(LinkedIn)上关注我们:
http://www.linkedin.com/company/huidagene

